「mRNAワクチン、がん、そして自己免疫疾患」への応用
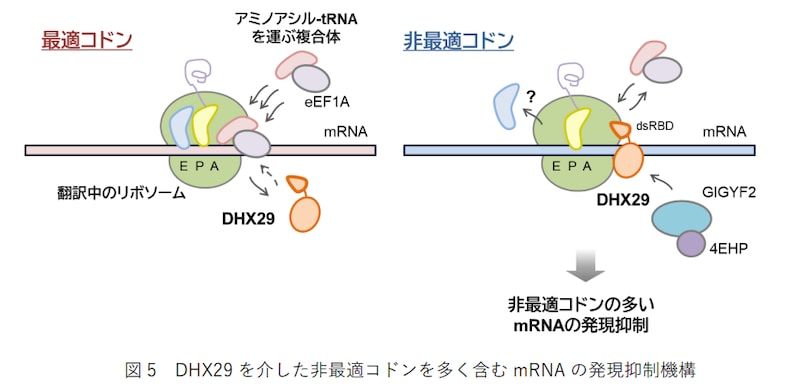
この発見は、基礎生物学の教科書を書き換えるだけにとどまりません。
私たちの未来の医療までも、静かに、しかし根本から変えてしまう可能性を秘めているのです。
まず最も直接的な影響を受けるのが、mRNAワクチンとmRNA医薬品の分野でしょう。
新型コロナウイルス禍で世界を救ったあの技術の本質は、人工的に作ったmRNA(タンパク質の設計図の写し)を体に注射し、体内でウイルスの目印を作らせて免疫を訓練する、というものでした。
この方法で効き目を決める大きな要素の一つは、注射されたmRNAが体の中でどれだけ長く生き延びられるかです。
必要とするmRNAの設計図のコドンにAやUが多いと、体内ですぐに分解されてしまい、十分な量の目印タンパク質が作られないまま、治療効果が尻すぼみに終わってしまいます。
ですが今回の発見を応用すれば話は変わります。
将来的には、DHX29の目をかいくぐりやすいスペル(優等生コドンばかりを集めた設計)でmRNAを書き直せば、少ない投与量でより長く効くワクチンや薬が作れるかもしれません。
これは現在、世界中の製薬会社が火花を散らしているmRNA医薬品開発レースの、ルール自体を書き換えかねない知見です。
次に期待されるのが、がん治療への応用です。
実はDHX29遺伝子に異常が見つかるがんの報告が、一部で出てきていました。
mRNAの品質管理が壊れることで、本来なら処分されるべき不良設計図のタンパク質が増えてしまい、それが細胞のがん化を後押ししている可能性がある――そんなシナリオが、今回の発見で現実味を帯びてきたのです。
この場合、もし何らかの手段でDHX29の機能を回復してやれば、遺伝子チェックが正常に戻り、がん化を押しとどめたり、がん細胞の増殖にブレーキをかけたりできるかもしれません。
さらにこのメカニズムの異常は、自己免疫疾患や神経変性疾患にまで顔を出し始めています。
「不良設計図のmRNA」が処刑を免れて細胞内に残り続けると、そこから余計なタンパク質が過剰に作られ、免疫系が自分の細胞を攻撃する引き金になったり、神経細胞の中に異常なタンパク質が蓄積して神経を壊してしまったりすると考えられるからです。
つまりDHX29は、一つの病気の原因というよりも、多くの難病を横断する「共通の急所」の有力な候補として浮上したわけです。
この共通の急所を狙い撃ちできる薬が作れれば、複数の病気に一気に効く治療薬が生まれる可能性さえあります。
同じ意味のはずのスペルに、命の設計図の寿命を決める隠された意味があった・・・
そしてその意味を読み取る番人は、あなたの細胞のなかで今この瞬間も、音もなく空いた席を探して歩き回っている。
日本主導の国際チームが引きずり出したこの事実は、生命がいかに繊細で、多重で、そして私たちの理解よりずっと巧妙に設計されているかを、教えてくれました。
参考文献
遺伝暗号の使い分けを認識する分子機構を解明―ヒト細胞における非最適コドンのセンサーを同定―
https://www.kyoto-u.ac.jp/ja/research-news/2026-03-23
元論文
Human DHX29 detects nonoptimal codon usage to regulate mRNA stability
https://doi.org/10.1126/science.adw0288
ライター
川勝康弘: ナゾロジー副編集長。 大学で研究生活を送ること10年と少し。 小説家としての活動履歴あり。 専門は生物学ですが、量子力学・社会学・医学・薬学なども担当します。 日々の記事作成は可能な限り、一次資料たる論文を元にするよう心がけています。 夢は最新科学をまとめて小学生用に本にすること。
編集者
ナゾロジー 編集部